ANA BOTTALLO
SÃO PAULO, SP (FOLHAPRESS) – Múltiplos fatores provocaram a morte da primeira pessoa no mundo a receber o transplante de um coração de porco geneticamente modificado. Além disso, vírus suínos detectados no órgão não se espalharam para outras partes do corpo do paciente.
A conclusão consta de um estudo, publicado no último dia 29 na revista The Lancet, feito pela equipe médica responsável pela cirurgia.
David Bennett, 57, tinha uma condição cardíaca que o levaria à morte caso não recebesse um transplante de coração. Com outras doenças crônicas, porém, ele não era elegível para um transplante de coração humano.
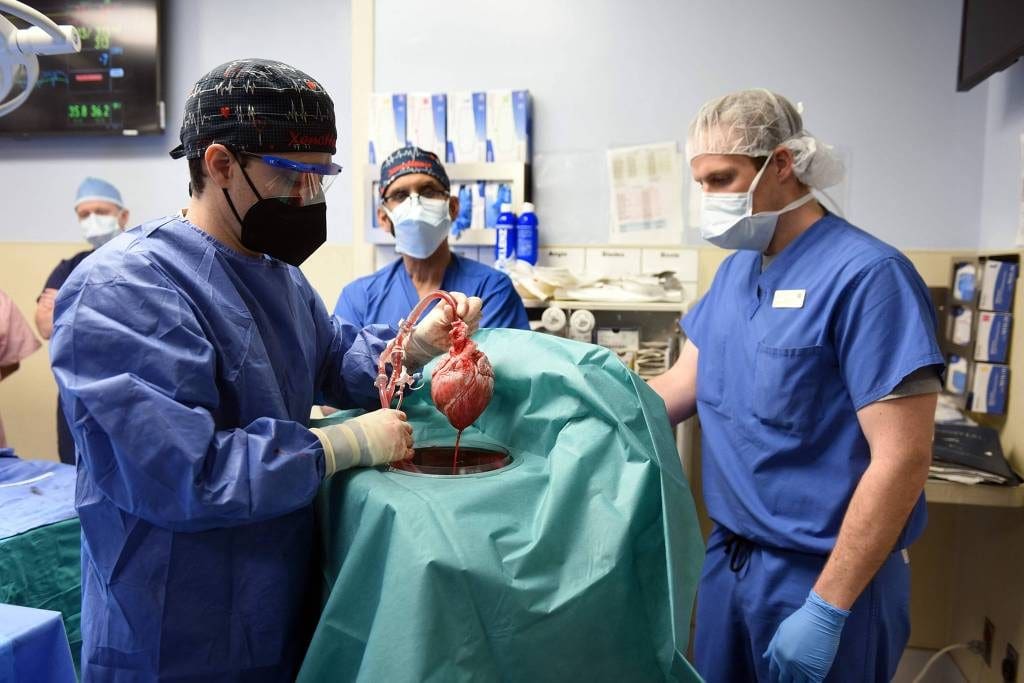
Em 7 de janeiro de 2022, ele passou por uma operação de oito horas no Centro Médico da Universidade de Maryland para receber o transplante de coração suíno.
O coração suíno foi geneticamente modificado para incluir genes humanos que tornam o órgão mais tolerável pelo nosso sistema imunológico. Outros genes suínos foram deletados para impedir o crescimento do órgão dentro do corpo e outras funções.
A equipe de pesquisadores divulgou no estudo as principais lições aprendidas com o primeiro xenotransplante (nome dado ao procedimento que ocorre com órgãos de outras espécies animais) feito em um paciente ainda vivo.
A ideia é que a pesquisa ajude a identificar possíveis falhas e aprimorar o caminho para novos procedimentos no futuro.
A causa da morte de Bennett foi uma parada cardíaca dois meses depois do procedimento.
Ao analisarem o órgão transplantado, os pesquisadores notaram endurecimento da parede do miocárdio, a musculatura que recobre o coração, danos múltiplos ao endotélio (parede mais fina e interna dos capilares sanguíneos) e inflamação do órgão, consequência provavelmente de uma resposta imune exacerbada desencadeada por uma possível rejeição ao órgão.
Como a saúde do paciente estava deteriorada, os médicos administraram imunoglobulina intravenosa (IVIG, na sigla em inglês) para tentar ajudar a recuperar o sistema imune debilitado. Durante a administração, porém, os anticorpos podem ter reconhecido o órgão como um invasor e provocado a resposta imune contra o próprio tecido cardíaco.
Além disso, foi detectada na análise genética do coração a presença de dois tipos de vírus suínos, o citomegalovírus suíno (PCMV) e o vírus da roséola suína (PRV), mas nenhum fragmento de DNA viral foi detectado em outros órgãos do paciente, o que descarta que uma provável infecção viral tenha causado a morte.
De acordo com os cientistas, é provável que os vírus, que estavam dormentes no órgão, tenham sido liberados da parede do coração após a ação exagerada do sistema imune do paciente. Com a chamada síndrome inflamatória, o vírus pode ter provocado ainda mais deterioração na parede cardíaca.
Um dos pontos levantados pelos autores no estudo é que não foi feito um teste na imunoglobulina intravenosa antes da administração ao paciente para investigar se haveria possibilidade de reação cruzada. Essa reação imune exacerbada poderia ter sido evitada caso células da veia aorta do porco tivessem sido testadas antes da cirurgia.
“É provável que a reação imune tenha sido provocada só após a injeção no paciente, já que detectamos também uma diminuição na expressão gênica dos genes que supostamente previnem a rejeição e uma elevada expressão de genes que regulam a ação inflamatória humana nas células endoteliais”, explicam os autores.
Os cientistas afirmam, porém, que Bennett foi “um herói” que voluntariou a própria vida à ciência, e esperam que o próximo paciente seja bem-sucedido. “Novos transplantes de porco geneticamente modificados em humanos podem melhorar nossa compreensão dos mecanismos de falha dos xenoenxertos e ajudar a lidar melhor com os procedimentos clínicos”, completam os autores.








